- 검색
| 소알호) 아스트라제네카 코로나19 백신 안전성 관련 서한 | |||
| 작성일 | 2021-05-10 | 조회수 | 700 |
|---|---|---|---|
|
아스트라제네카 코로나19 백신 안전성 관련 서한 (2021. 5. 7)
 1.
코로나19 백신의 종류 A.
불활성화 백신: Sinovac B.
단백질 아단위백신(subunit vaccine): Novavax C.
아데노바이러스 벡터백신: 아스트라제네카, 얀센, 스푸트니크 V D.
mRNA 백신:
화이자, 모더나
2.
아스트라제네카 백신의 합병증 A.
대부분의 이상반응은 경미하고 예방 접종 후 수 일 이내에 소실되나 7일까지 지속되는 경우가 국소 반응은 4%, 전신 반응은 13%까지 보고 되고 있다. B.
자주 보고되는 이상 반응은 접종부위 압통(60% 이상), 접종부위 통증, 두통, 피로감
(50% 이상), 근육통,
권태감 (40% 이상), 발열, 오한 (30% 이상), 관절통, 메스꺼움 (20% 이상) 등이
있다. C.
드물게 발생하는 이상 반응으로는 림프선염, 식욕감소, 어지러움, 복통, 다한증, 소양증, 발진 등의 증상이 보고 되었다. D.
유럽의약품청에서는 백신 유도 혈전호발성 면역 혈소판 감소증(Vaccine Induced Prothrombotic Immune Thrombocytopenia, VIPIT)을 매우 드물게 발생할
수 있는 부작용으로 등록하였다.
3.
COVID-19의 위험도와 아스트라제네카 백신의
위험도 비교 A.
유럽의약품청의 보고에 따르면 아스트라제네카 백신 접종에 의한 혈전증 발생의 위험도는 연령에
따라 차이를 보이며, 인구 10만명 당 20-29세에서는 1.9건,
30-39세에서는 1.8건, 40-49세에서는
2.1건, 60-69세에서는 1건, 70-79세에서는 0.5건, 80세 이상에서는 0.4건이 발생하였다.
B.
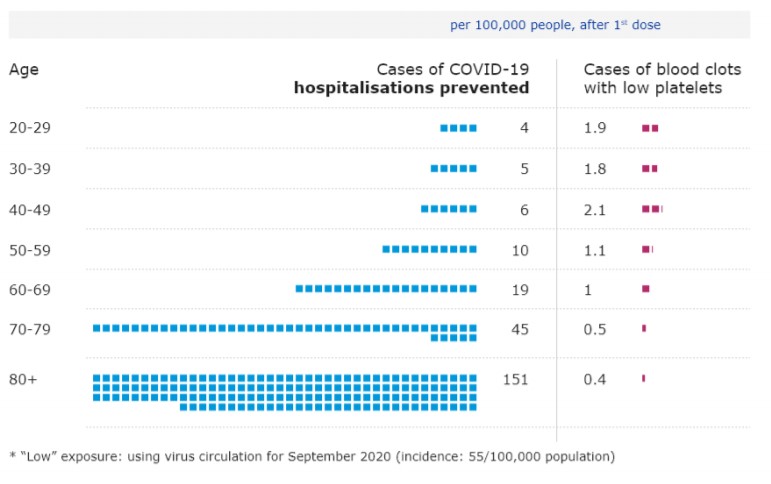
아스트라제네카 백신 접종으로 예상되는 입원환자 발생의 예상 감소율은 한달 동안 코로나감염증
환자의 발생률이 인구 10만명당 55명 정도의 수준으로 계산이
되었을 때, 인구 10만 명당 20-29세 4건, 30-39세
5건, 40-49세 6건, 50-59세 10건, 60-69세
19건, 70-79세 45건, 80세 이상 151건으로 나타났다(Figure
1).
Figure 1 감염수준이 낮은 상황에서 아스트라제네카 백신 접종에 따른 입원 예방과 혈전증 발생의 위험도 비교
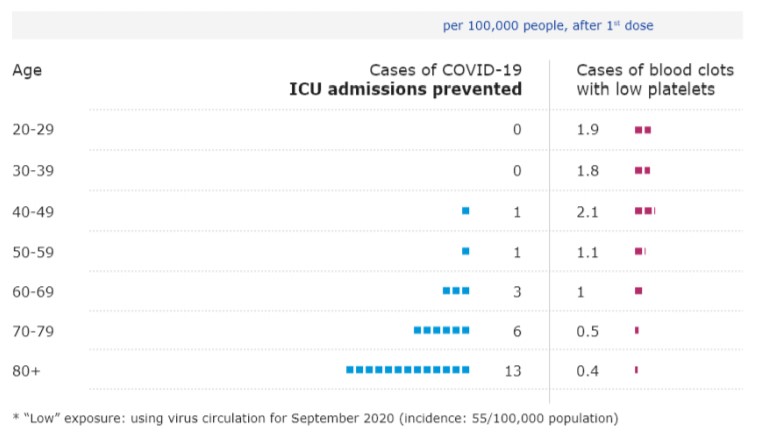
C. 접종으로 예상되는 중환자실 입실 발생의 예상 감소율은 인구 10만 명당 20-29세 0건, 30-39세 0건, 40-49세
1건, 50-59세 1건, 60-69세 3건, 70-79세
6건, 80세 이상 13건으로
나타났다(Figure 2).
Figure 2 감염수준이 낮은 상황에서 아스트라제네카 백신 접종에 따른 중환자실 입실 예방과 혈전증 발생의 위험도 비교
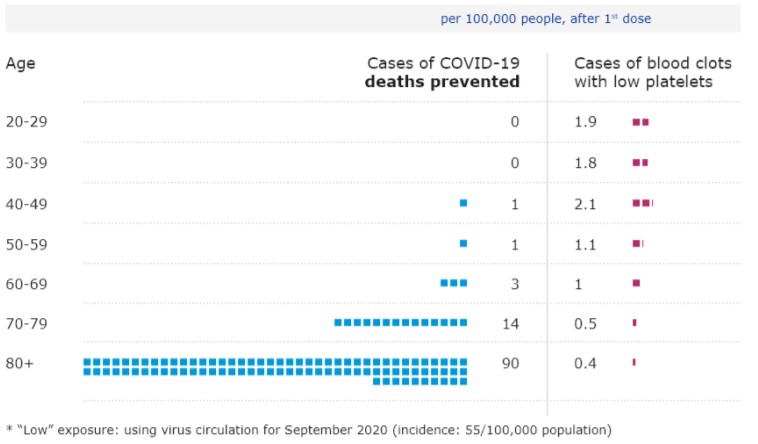
D. 접종으로 예상되는 사망자 발생의 예상 감소율은 인구 10만
명당 20-29세 0건,
30-39세 0건, 40-49세 1건, 50-59세 1건, 60-69세 3건, 70-79세
14건, 80세 이상 90건으로
나타났다(Figure 3).
Figure 3 감염수준이 낮은 상황에서 아스트라제네카 백신 접종에 따른 사망률 감소와 혈전증 발생의 위험도 비교
4. 결론
A. 유럽의약품청에서는 아스트라제네카 백신의 유익성을 감염 수준이 낮은 상황(한달 평균 감염자 10만 명당 55명), 중간 단계 감염 수준 상황(한달 평균 감염자 10만명당 401명), 감염 수준이 높은 상황 (한달 평균 감염자 10만명당 886명)으로 분류하여 보고하였으며, 중간 단계와 높은 단계 감염 수준에서는 더 높은 비율의 입원, 중환자실 입실, 사망률의 감소가 예상된다고 보고하였다. B.
유럽의약품청에서는 2차 접종의 시기를 더 늦추는
방법, 2차 접종을 하지 않는 방법, mRNA 백신을 2차 접종으로 하는 방법을 모두 고려 하였으나 아스트라제네카 백신 접종을 4-12주
사이에 2차 접종하는 것을 최종적으로 권고 하였다. C.
국내의 코로나19 감염의 유행 수준이 유럽 또는 미국의
상황과는 다르기 때문에 아스트라제네카 백신 접종의 위험도와 이익을 충분히 고려하여 접종 여부를 결정할 필요가 있다.
참고문헌 1.
Use of Vaxzevria to prevent
COVID-19 - Article-5(3) procedure: Assessment report EMA/CHMP/214855-2021 (2021년 4월 23일) 2.
Annex to Vaxzevria Art.5.3 -
Visual risk contextualization EMA/234525/2021 (2021년 4월
23일)
3. 코로나 19 예방접종 후 발생한 혈소판 감소증 동반 혈전증 관련 안내서(초판) 질병관리청 2021년 4월.
|
|||
- 다음글
- [대한의학회] 대한의사협회 회비 납부 협조 요청 2021-05-13
- 이전글
- 소알호) 2021년 대한소아청소년과학회 분과전문의 자격시험 안내 2021-05-06

 > 학회소식 > 공지사항
> 학회소식 > 공지사항