- 검색
| 소알호) 코로나19백신개발과 임상시험 | |||
| 작성일 | 2020-08-25 | 조회수 | 839 |
|---|---|---|---|
|
회원 여러분, 안녕하십니까? 코로나19의 재확산과 국내 의료 정책의 혼선으로 어려움이 많은 상황입니다. 이전에 없던 감염병의 진행과 미래를 예측할 수 없지만 국내외의 많은 의료진은 환자의 안전과 회복을 위해 진료에 임하며 코로나19의 치료제와 백신 개발을 위한 연구를 지속하고 있습니다. 코로나19 백신 개발과 임상시험에 대한 결과들이 보고되고 있어 이에 대한 최신 지견을 공유하고자 합니다. 우리 학회는 소아청소년의 건강을 위해 회원들과 함께 노력하겠습니다. 2020. 8. 25 대한 소아알레르기 호흡기학회 이사장 홍수종/홍보사회위원회 드림
2019년 말 이후 SARS-CoV-2가 세계적으로 확산되면서, 120개 이상의 SARS-CoV-2 candidate 백신이 개발될 정도로 전 세계적으로 백신 개발에 전력을 다하고 있다. 현재 임상 시험에 들어간 SARS-CoV-2 백신의 원리는 크게 세 가지 기전으로 분류된다. 첫째, 재조합 바이러스 벡터가 내인성 항원으로 작용하여 프로테아좀에서 가공된 후 MHC1에 표지 되어 toxic T-cell에 의한 세포매개 면역반응을 일으키는 것이다. 둘째, DNA 백신으로 숙주세포 내에서 전사와 번역 되는 것이다. 그 이후 MHC1 경로로 가거나 숙주 세포 외부로 이동하여 외인성 항원으로 작용하여 MHC2에 표지 되어 T helper cell의 체액매개 면역반응을 일으키는 것이다. 셋째, mRNA 백신으로 숙주세포의 내포 작용을 통해 들어가 두번째 언급한 DNA 백신과 같은 MHC2 경로를 통해 체액매개 면역반응을 일으킨다 (Figure. 1).
Figure. 1. Mechanism of action of various vaccine candidates: Vaccination strategies to combat novel corona virus SARS-CoV-2. Life Sciences Volume 256, 2020, 117956
여러 백신 관련 연구 중 SARS-CoV-2 백신들에 대한 두 개의 임상 시험 보고를 공유하고자 한다.
An mRNA Vaccine against SARS-CoV-2 — Preliminary Report
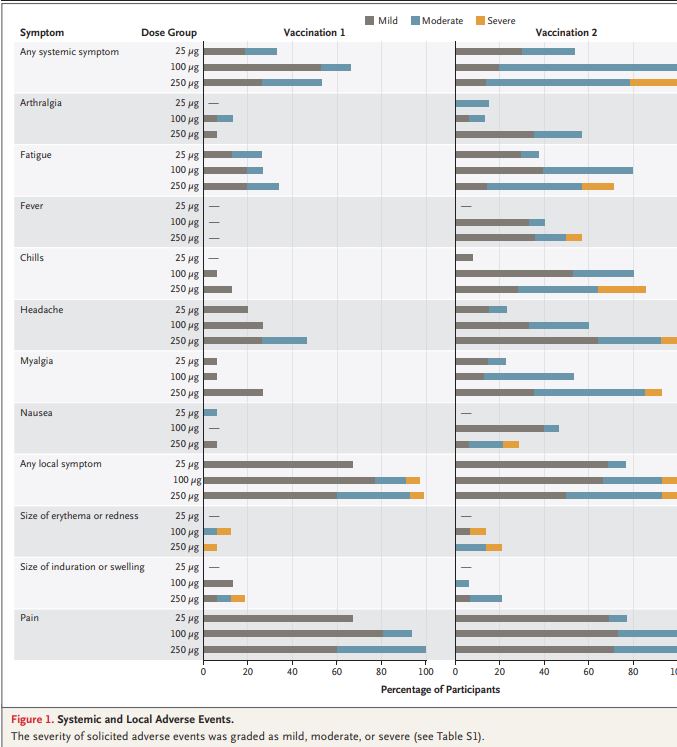
SARS-CoV-2 바이러스는 스파이크 단백질을 미리 형성하여 사람의 수용체 단백질과 결합하여 침투하는 기전을 가진다. mRNA-1273 candidate 백신은 mRNA 기반 백신으로, SARS-CoV-2의 스파이크 S 단백질을 암호화하여 체내에서 이에 대항하는 항체를 생성하도록 하여 침투를 차단하는 원리이다. 본 mRNA-1273 candidate 백신의 안전성과 면역유전성을 평가하기 위하여 18세에서 55세 사이의 건강한 성인 45명을 대상으로 한 연구가 이루어졌다. mRNA-1273으로 28일 간격으로 두 번의 접종을 한 phase 1, dose-escalation, open-label trial 이였으며, 25 μg, 100 μg, 250 μg의 용량으로 각 그룹에는 15명이 참가하였다. 첫 접종 뒤 항체 반응은 day 29 시점에서 enzyme-linked immunosorbent assay (ELISA) 로 측정한 anti–S-2P antibody 평균 값이 40,227 (25-μg group), 109,209 (100-μg group), 213,526 (250-μg group)으로 용량이 증가할수록 더 높았다. 그리고 두 번째 접종 이후 항체 반응은 day 57 시점에서, anti–S-2P antibody 평균값이 299,751 (25-μg group), 782,719 (100-μg group), 1,192,154 (250-μg group)로 세 그룹 모두 첫 항체 반응보다 증가하였으며, 접종 용량이 증가할수록 더 높았다. 2차 접종 후, 모든 참가자에서 혈청 중화항체가 검출되었다. 연구 참가자들의 절반 이상 발생한 부작용으로는 피로, 오한, 두통, 근육통, 주사 부위의 통증 등이 있었다. 그리고 주사 부위의 통증과 전신 이상반응은 2차 접종 이후에서 고용량 (250-μg) 그룹에서 더욱 흔했고, 고용량 (250μg) 그룹의 참가자 3명(21%)이 하나 이상의 심각한 이상반응을 보고했다 (Figure 1).
결론적으로 mRNA-1273 candidate 백신은 모든 참여자에게 anti–SARS-CoV-2 면역반응을 유도하였으며, trial-limiting safety concern은 확인되지 않았다.
Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomised controlled trial
ChAdOx1 nCoV-19 vaccine
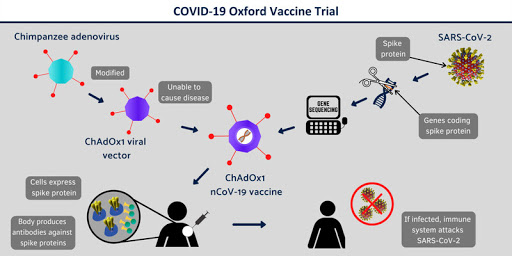
영국 제너연구소는 재조합 DNA 기술을 사용해 SARS-CoV-2 항원을 만들고, 이를 영장류 아데노바이러스 벡터 내에 삽입하는 방법으로 'ChAdOx1 nCoV-19'를 개발했다. 올해 1월 중순 SARS-CoV-2의 유전자 서열이 이용 가능해지면서 백신 개발을 하고 있으며, 본 연구에서는 ChAdOx1 nCoV-19 백신의 안전성, 면역 반응성과 면역 유전성을 평가했다. 2020년 4월 23- 5월 21일 사이에 총 1077명의 참가자가 등록되었다. 영국 5개 시험장에서 ChadOx1 nCoV-19로 1/2단계, 단일 무작위 제어 실험을 했는데, SARS-CoV-2 스파이크 단백질을 메닌코코칼주게이트 백신(MenACWY)과 비교하였다.
SARS-CoV-2 감염 이력이나 또는 COVID-19 유사 증상들이 전혀 없는 18~55세의 건강한 성인을 대상으로, 임의로 ChAdOx1 nCoV-19 (a dose of 5×10¹⁰ viral particles) 또는 MenACWY를 받도록 배분하였다. 그리고 10명의 참가자는 무작위로 ChadOx1 nCoV-19 prime-boost 그룹에 배정되어 1차 투여 8일 후에 booster 백신이 투여되는 총 2회 투여를 하였다. 세포매개 및 혈장매개 반응성을 백신 접종 이전과 백신 접종 이후 총 두 번 측정하였다. 접종 후 28일 동안 안전성도 같이 평가되었다.
ChadOx1 nCoV-19 그룹에서 접종 이후 국소적, 전신적인 반응이 더 흔하였으나 통증, 열감, 오한, 근육통, 두통 증상은 예방적 파라세타몰을 사용함으로써 감소되었으며(all p<0·05), 심각한 부작용은 없었다.
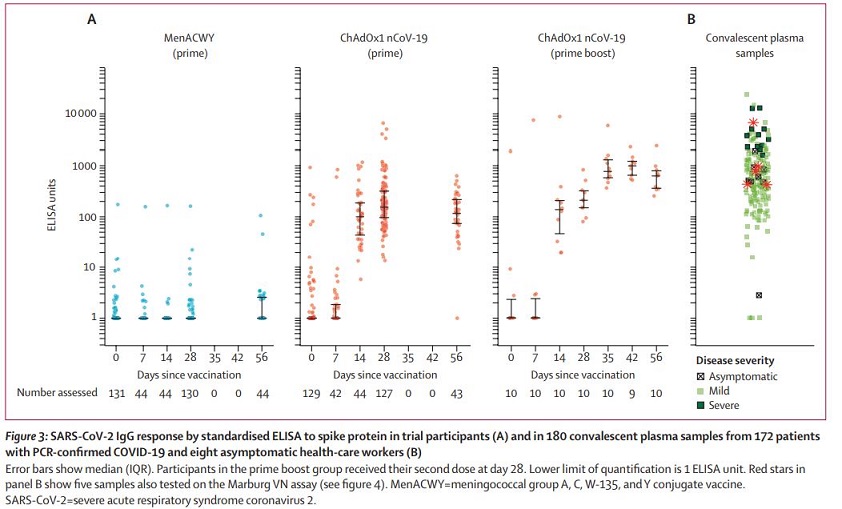
ChadOx1 nCoV-19 그룹에서 spike-특이 T세포 반응은 day 14에 정점을 보였다(median= 856 spot-forming cells per million peripheral blood mononuclear cells, n=43). Anti-spike IgG 반응은 day 28 (median=157 ELISA units [EU], n=127), 까지 상승하였으며, 2차 접종 투여 후 더 증가하였다 (median=639 EU, n=10)(Figure 3).
SARS-CoV-2에 대한 중화항체 반응은 single dose 투여한 35명의 참가자 중 MNA80으로 측정했을 때는 32명(91%), PRNT50으로 측정했을 때 35명(100%)에서 검출되었다. Booster dose이후 모든 참가자는 neutralising activity를 가졌다. 중화 항체 반응은 ELISA에 의해 측정된 항체 농도와 상관 관계를 가졌다(R²=0·67 by Marburg VN; p<0·001). 본 연구에서 ChadOx1 nCoV-19 백신은 허용 가능한 안전성을 보여주었고, boosting 접종은 항체 반응을 증가시켜 single dose보다 더 유용할 것으로 생각된다.
출처 Jackson LA. An mRNA vaccine against SARS-CoV-2. Preliminary Rport. N Eng J Med 2020 Jul 14:NEJMoa2022483. doi: 10.1056/NEJMoa2022483 Folegatti PM. Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomized controlled trial. Lancet 2020;396:467-78
|
|||
- 다음글
- 2020년 대한의사협회 제37차 온라인종합학술대회 홍보요청 2020-09-10
- 이전글
- 소알호) 제251회 대한 소아알레르기 호흡기학회 월례 학술집담회 (온라인) 2020-08-18

 > 학회소식 > 공지사항
> 학회소식 > 공지사항